Алкeны
АЛКЕНЫ (олефины, этиленовые углеводороды), ненасыщенные алифатические углеводороды общей формулы СnН2n; содержат одну двойную связь С=С. Первый член гомологического ряда этилен (этен) Н2С=СН2. Для алкенов, начиная с бутена С4Н8, наряду с изомерией углеродного скелета и положения двойной связи, возможна геометрическия изомерия (смотри Изомерия). В алкенах атомы углерода при двойной связи имеют sp2-гибридизацию.
Низшие алкены - этен, пропен и бутены газы, алкены состава С5-С18 - бесцветные жидкости, высшие алкены - твёрдые вещества. Алкены практически не растворяются в воде, ограниченно - в спиртах; хорошо растворяются в углеводородах и их галогенпроизводных, простых и сложных эфирах.
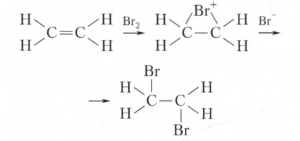
Алкены легко вступают в реакции электрофильного присоединения по двойной связи с галогеноводородами, галогенами, кислотами и др., протекающие главным образом через стадию образования мостикового иона, например;
Реклама
Присоединение электрофильных реагентов протекает в соответствии с Марковникова правилом. При взаимодействии алкенов с формальдегидом образуются диолы или 1,3-диоксаны (смотри Принса реакция), при гидроформилировании - альдегиды. Гидратацией алкенов в присутствии кислотных катализаторов (например, Н2SО4) получают спирты; так, гидратацией этена и пропена в промышленности получают этиловый и изопропиловый спирты. Алкены способны алкилировать алканы с образованием алканов разветвлённого строения, которые применяют в качестве высокооктановых добавок к моторным топливам. При алкилировании бензола этеном образуется этилбензол, пропеном - кумол (смотри Алкилирование, Фриделя - Крафтса реакция). Алкены вступают в реакции радикального присоединения по двойной связи. При взаимодействии алкенов со свободным радикалом может происходить полимеризация по цепному механизму или присоединение, например:
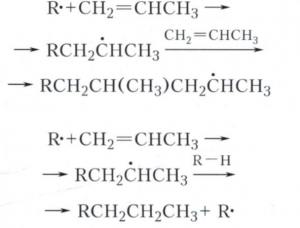
Соотношение между продуктами полимеризации и присоединения зависит от природы алкенов и реагента, а также от их концентрации. Реакции нуклеофильного присоединения к алкенам протекают только с сильными нуклеофилами, например с С4Н9Li. К реакциям нуклеофильного присоединения относится анионная полимеризация алкенов с применением катализаторов Циглера - Натты. В промышленности таким способом получают высокомолекулярный полиэтилен, стереорегулярный изотактический полипропилен, этилен-пропиленовые каучуки и др. При окислении алкенов в зависимости от условий реакции образуются различные продукты. В слабощелочной среде KMnО4 окисляет алкены до гликолей, в кислой среде происходит расщепление двойной связи и образование кетонов и карбоновых кислот. В присутствии Ag2О при 200-300°С кислород взаимодействует с алкенами с образованием эпоксисоединений, в промышленности таким способом получают этиленоксид и пропиленоксид. При действии на алкены надкислот образуются эпоксиды (смотри Эпоксидирование). При каталитическом гидрировании алкенов образуются соответствующие алканы.
В промышленности алкены получают переработкой нефтепродуктов и природного горючего газа. Низшие алкены состава С2-С4 получают пиролизом прямогонного бензина, этана, пропана или газойля; пропен и бутен - каталитическим крекингом вакуумного газойля (смотри Пиролиз нефтяного сырья). Неразветвлённые алкены состава С6-С20 получают термическим крекингом парафиновой фракции нефти, содержащей нормальные алканы. В лабораторных условиях алкены получают следующими способами: дегидратацией спиртов; дегидрогалогенированием галогеналканов; разложением четвертичных аммониевых оснований (смотри Гофмана реакции); гидрированием ацетиленовых углеводородов или дегидрированием алканов; цис-алкены получают взаимодействием альдегидов или кетонов с алкилиденфосфоранами (смотри Виттига реакции).
Алкены — основные исходные реагенты в химической промышленности. Из этилена и пропилена получают полимеры и эластомеры, эпоксисоединения, дихлорэтан, винилхлорид, этанол, изопропанол, пропанол и др. Изобутилен - сырьё для получения бутилкаучука, изопрена, трет-бутанола.
Его сополимеры с бутенами применяют как присадки к маслам и герметики. Алкены состава С10-С16 используют в синтезе ПАВ, а также для получения высших спиртов.
Лит.: Робертс Дж., Касерио М. Основы органической химии. М., 1978. Т. 1; Общая органическая химия. М., 1981. Т. 1.
В. Н. Кошелев.