Ксантогенаты
КСАНТОГЕНАТЫ (от греческого ξανθός – жёлтый и γεννάω – рождать, производить) (дитиокарбонаты, ксантаты), соли и эфиры ксантогеновых кислот. Общая формула ксантогенатов:
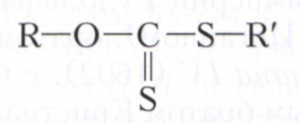
(R – органический радикал, R’ – металл, алкил или арил). В отличие от нестойких ксантогеновых кислот, ксантогенаты – устойчивые соединения. Представляют собой (в зависимости от природы заместителей R и R’) маслянистые жидкости или кристаллические вещества от жёлтого до жёлто-красного цвета с неприятным запахом. Стабильность ксантогенатов повышается с увеличением молекулярной массы и объёма заместителей. Ксантогенаты щелочных металлов растворяются в воде, спиртах, ацетоне, пиридине, ацетонитриле; ксантогенаты тяжёлых металлов растворяются в хлороформе, метиленхлориде, тетрагидрофуране, бензоле. Ксантогенаты щелочных металлов под действием влаги при нагревании разлагаются, например ксантогенат калия – на спирт (или фенол), К2CS3, CS2 и К2СО3. Эфиры ксантогеновых кислот при нагревании разлагаются с образованием ненасыщенного углеводорода – реакция Чугаева (или ксантогеновая), например:
Реклама
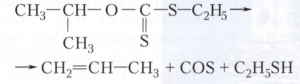
ксантогенаты щелочных металлов получают действием сероуглерода CS2 на щелочные растворы спиртов, крахмала, целлюлозы, фенолов или простых эфиров. Эфиры ксантогеновых кислот синтезируют алкилированием ксантогената щелочных металлов или взаимодействием последних с ароматическими диазосоединениями. Среди ксантогенатов металлов наибольшее значение имеют алкилксантогенаты (ускорители вулканизации каучуков, флотореагенты для извлечения из руд сульфидов тяжёлых металлов, полупродукты в производстве инсектицидов, фумиганты) и ксантогенаты целлюлозы. Эфиры ксантогеновых кислот являются полупродуктами органического синтеза.
Лит.: Органические реакции. М., 1965. Сб. 12; Общая органическая химия. М., 1983. Т. 5.
Ю. Н. Огибин.