Краун-эфиры
КРАУН-ЭФИРЫ (краун-соединения), макрогетероциклические соединения, содержащие в цикле свыше 11 атомов, из которых не менее 4 - гетероатомы (О, N, S), связанные между собой этиленовыми мостиками. Молекулы краун-соединений имеют конформацию короны, что и определило название веществ этого класса (от английского crown - корона). Впервые синтезированы Ч. Педерсеном в 1967 году. За открытие и исследование свойств макрогетероциклических соединений Ч. Педерсену, Д. Краму и Ж. М. Лену присуждена Нобелевская премия (1987).
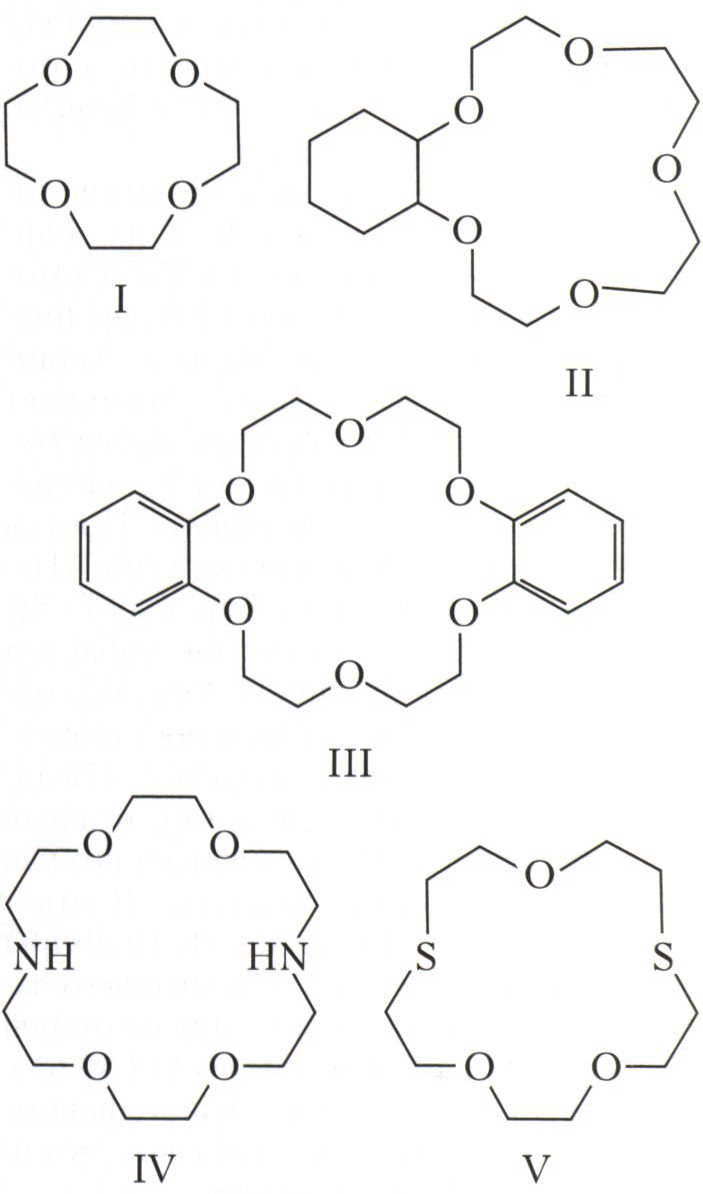
Структура простейшего краун-эфира представлена формулой I. Получены краун-соединения, содержащие в цикле другие гетероатомы (Р, Si, As), функциональные группы (сложноэфирные и пр.), а также конденсированные с одним или несколькими бензольными, циклогексановыми кольцами (в том числе замещёнными). В тривиальных названиях краун-эфира общее число атомов в цикле и число гетероатомов обозначают цифрами, которые ставят соответственно перед и после слова «краун»; например, 12-краун-4 (формула I), циклогексано-15-краун-5 (II), дибензо-18-краун-6 (III), 1,10-диаза-18-краун-6 (IV), 1,7-дитиа-15-краун-5 (V).
Реклама
Краун-эфиры - вязкие жидкости или кристаллические вещества; растворяются в воде и в большинстве органических растворителей. Химические свойства определяются природой гетероатома и функциональных групп. Краун-эфиры образуют макроциклические комплексные соединения как с катионами, так и с нейтральными молекулами. В комплексах краун-эфира с катионами металлов (щелочных, щёлочноземельных и др.) катион включается во внутримолекулярную полость краун-эфира и удерживается там благодаря ион-дипольному взаимодействию с гетероатомами (один из способов расположения катиона металла в полости краун-эфира представлен формулой VI). Селективность связывания и устойчивость образуемых краун-эфиром комплексов зависит от ряда факторов – геометрического соответствия размеров внедряющейся частицы и полости макроцикла, природы растворителя, хелатного и макроциклических эффектов, заряда внедряющейся частицы, природы противоиона и пр. За счёт комплексообразования краун-эфиры повышают растворимость солей щелочных и щёлочноземельных металлов в малополярных растворителях; пример - образование малинового бензола и оранжевого бензола (окислительных реагентов) при растворении в бензоле соответственно KMnО4 или К2Cr2О7 в присутствии краун-эфира. Щелочные металлы в присутствии краун-эфира растворяются в координирующих органических растворителях; интенсивный синий цвет образующихся растворов объясняется присутствием в них сольватированной формы свободных электронов (получаемый раствор является восстановительным реагентом). Краун-эфиры способны селективно экстрагировать ионы металлов и некоторые органические соединения (амины, аминокислоты и др.) из водной фазы в органическую, энантиоспецифически связывать хиральные молекулы (в частности, протонированные формы аминокислот). За счёт влияния на ионную и субстратную проницаемость биологических мембран, на ферментные системы и другие биохимические процессы краун-эфиры проявляют различные виды биологической активности.
Краун-эфир получают в основном конденсацией дигалогеналканов или диэфиров n-толуолсульфокислоты (дитозилатов) с полиэтиленгликолями, внутримолекулярной циклизацией монотозилатов полиэтиленгликолей, циклоолигомеризацией этиленоксида. Конденсацию проводят в присутствии катионов металлов (чаще К+, Cs+), внутримолекулярную циклизацию - в условиях высокого разбавления.
Краун-эфир широко используют в научных исследованиях как доступные и разнообразные модели при изучении сложных природных супрамолекулярных систем. С помощью краун-эфира можно избирательно выводить из организма ионы тяжёлых металлов или вводить малые количества нужных ионов или молекул. Краун-эфиры применяют для концентрирования, разделения, очистки и регенерации металлов, в том числе лантаноидов, для разделения нуклидов, энантиомеров; для создания ионоселективных датчиков и мембран; в межфазном катализе и для ускорения реакций, проходящих с участием анионов; как лекарственные препараты, пестициды, антидоты.
Лит.: Хираока М. Краун-соединения. Свойства и применения. М., 1986; Химия комплексов «гость-хозяин» / Под редакцией Ф. Фегтле, Э. Вебера. М., 1988.
О. Б. Рудаков.