Альдегиды
Смотрите также:
АЛЬДЕГИДЫ [от новолатинского al(cohol)dehyd(rogenatum) - алкоголь, лишённый водорода], органические соединения, содержащие альдегидную группу; общая формула RCH=О (R - водород или органический радикал); относятся к карбонильным соединениям. Первый член гомологического ряда - формальдегид - газ, остальные альдегиды - жидкости, реже твёрдые вещества. Низшие альдегиды имеют резкий запах, смешиваются с водой в любых соотношениях; с увеличением молекулярной массы растворимость альдегида в воде падает. Большинство альдегидов хорошо растворимы в этиловом спирте.
Альдегиды характеризуются высокой реакционной способностью, легко окисляются кислородом воздуха по свободнорадикальному механизму в соответствующие кислоты (промежуточный продукт пероксикислоты):
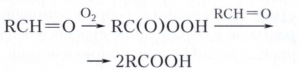
Альдегиды восстанавливаются в первичные спирты под действием водорода (катализатор - платина или никель), LiAlH4 или NaBH4, например: NaBH4 + 4СН2=О + 3Н2О→4СН3ОН + NaH2ВО3. Под действием амальгамы цинка в концентрированной соляной кислоте идёт восстановление альдегидов в соответствующие углеводороды (Клемменсена реакция). В присутствии щелочей происходит окислительно-восстановительное диспропорционирование альдегидов с образованием соответствующих спиртов и кислот (Канниццаро реакция). Простейший диальдегид - глиоксаль - легко подвергается внутримолекулярной окислительно-восстановительной реакции с образованием гликолевой кислоты НОСН2СООН. Нуклеофилы присоединяются к карбонильной группе или замещают в ней атом кислорода. Альдегиды со спиртами в кислой среде образуют ацетали RCH(OR’)2, с циановодородом в присутствии основания - гидроксинитрилы (циангидрины) RCH(OH)CN, с первичными аминами - шиффовы основания (азометины) RCH=N—R’. Замещённые амины, такие, как гидразин, гидроксиламин, фенилгидразин, вступают в реакцию с альдегидами подобно первичным аминам с образованием соответственно гидразонов RHC=N—NH2, оксимов RHC=NOH и фенилгидразонов RHC=N—NH—С6Н5. Взаимодействие альдегидов со вторичными аминами приводит к образованию енаминов RR’С=CHNRR’. Реакцию присоединения NaHSО3 к альдегидам с образованием кристаллического, так называемого бисульфитного, соединения RCH(ОН)SО3Na используют для очистки альдегидов (с последующей регенерацией нагреванием с раствором соды или с разбавлением кислотой). Важное значение имеет Гриньяра реакция, позволяющая получать из альдегидов первичные и вторичные спирты. Низшие альдегиды легко полимеризуются. Взаимодействие с другими альдегидами и кетонами называется альдольно-кротоновой конденсацией, например: RCH2CHO+ R’CH2CHO→RCH2CH(ОН)CH(R’)CH=О→ RCH2CH=С(R’)CH=О (смотри Альдольная конденсация, Кротоновая конденсация). Ароматические альдегиды легко вступают в подобную реакцию с ангидридами карбоновых кислот (реакция Перкина): ArCHO+(СН3СО)2О→ArCH=СНСООН (Ar - арильный радикал); алифатические и ароматические альдегиды с эфирами малоновой кислоты (Кнёвенагеля реакция). Важное значение имеет взаимодействие альдегидов с алкилиденфосфоранами, в результате которого образуются алкены преимущественно в виде Е-изомера: R2С=Р(С6Н5)3 + R’CH=О→R2С=CHR’ + (С6Н5)3Р=О (смотри в ст. Виттига реакции). Качественными реакциями на альдегиды являются образование «серебряного зеркала» при взаимодействии альдегидов с ионами серебра в аммиачном растворе и образование красного осадка оксида меди(1) при взаимодействии альдегидов с реактивом Фелинга (смотри Органических веществ анализ).
Реклама
Наиболее распространённый промышленный метод получения альдегидов - каталитическое дегидрирование спиртов. Альдегиды получают также каталитическим восстановлением карбоновых кислот, взаимодействием алкенов с СО и Н2 (смотри Гидроформилирование), присоединением воды к ацетилену в присутствии солей ртути (Кучерова реакция).
Альдегиды применяют в промышленном органическом синтезе спиртов и их производных, карбоновых кислот, гетероциклических соединений и др. На основе альдегидов получают полимерные материалы, такие, как феноло-формальдегидные, полиформальдегидные и другие смолы, фармацевтические препараты, душистые вещества. В природе альдегиды обнаружены в эфирных маслах (цитраль, ванилин и др.), зелёных листьях (2-гексеналь).
См. также Акролеин, Ацетальдегид, Бензальдегид, Хлораль.
Лит.: Терней А. Современная органическая химия: В 2 т. М., 1981; Общая органическая химия. М., 1982. Т. 2; Органикум: В 2 т. М., 1992.
М. М. Кабачник.